O Epstein-Barr vírus (EBV) é um DNA vírus da família Herpesviridae que está presente de forma latente em 95% da população mundial. É transmitido por gotículas de saliva que alcançam a faringe e infectam os linfócitos B, promovendo uma infecção persistente com reativações periódicas. Dessa forma, esse vírus é suspeito de ser um forte fator ambiental na etiologia de doenças autoimunes, uma vez que suas proteínas virais estão envolvidas na alteração do sistema imune do hospedeiro e perca da autotolerância1- 3.
Na literatura, é observada a associação do vírus com as doenças autoimunes: lúpus eritematoso sistêmico (LES), síndrome de Sjögren, artrite reumatoide, miosite, miastenia gravis, artrite idiopática juvenil e esclerose múltipla1-3. Entretanto, não são encontradas relações específicas de causalidade entre o EBV e a dermatopolimiosite (DM), mas é possível identificar o aumento da carga viral e a predominância de anti-VCA nos indivíduos portadores de DM em comparação com indivíduos não portadores, o que sugestiona seu potencial envolvimento na patogênese dessa doença4.
Neste artigo, é exposto um caso de associação entre EBV e dermatopolimiosite em uma criança de cinco anos, no qual há elevação da carga viral em consonância com piora do quadro reumatológico, fato que urge atenção médica para suspeição de infecção por EBV e o correto manejo desses pacientes.
RELATO DE CASO
Menina, 5 anos, com edema facial e lesões de pele eritemato-descamativas em regiões extensoras nos membros superiores e inferiores. A vacinação estava atualizada e apresentava mãe portadora de lúpus eritematoso sistêmico diagnosticado desde a adolescência. Durante acompanhamento, a genitora retornou referindo piora da paciente, queixando-se de febre intermitente, infecção de via aérea superior e piora das lesões de pele com fraqueza muscular e dificuldade ao deambular e sentar há aproximadamente três semanas.
Ao exame físico encontrava-se com estado geral regular, chorosa, irritada, edema facial, enduração da pele, faringoamigdalite, adenomegalias cervical, axilar, inguinal e hepatomegalia. Pele com máculas eritematosas descamativas e pruriginosas em membros superiores e inferiores (Figura 1) e sobre as articulações metacarpofalangeanas e interfalangeanas (Sinal de Gottron) (Figura 2), fraqueza da musculatura pélvica, movimento coxofemoral limitado, marcha anserina e artralgia em joelhos e tornozelos.
 Figura 1. Máculas eritematosas descamativas em membros inferiores.
Figura 1. Máculas eritematosas descamativas em membros inferiores. Figura 2. Máculas eritematosas descamativas sobre as articulações metacarpofalangeanas e interfalangeanas (sinal de Gottron).
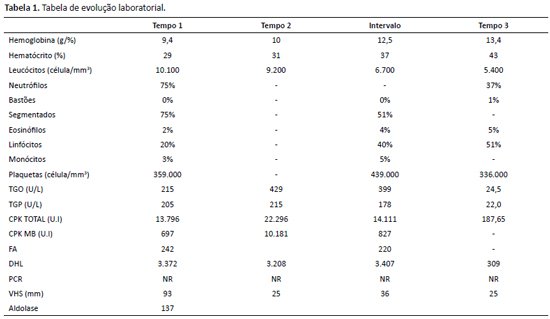
Figura 2. Máculas eritematosas descamativas sobre as articulações metacarpofalangeanas e interfalangeanas (sinal de Gottron).Exames complementares mostrando: anemia, linfocitose, TGO e TGP elevados, sorologia para o vírus Epstein-Barr positiva (IgM e IgG); CPK total, CPK-MB, fosfatase alcalina, desidrogenase lática, VHS e aldolase elevados (vide Tabela 1 - tempo 1); FAN reagente de padrwão nuclear com granulação fina tipo pontilhado maior que 1:1280; anti-DNA não reagente; anticorpos heterófilos reagentes; ultrassonografia de abdômen total: hepatomegalia moderada com presença de linfonodos periaórticos de aspecto reacional.
Internada em hospital pediátrico foi submetida à corticoterapia sem melhora do quadro, evoluindo com piora clínica e laboratorial (vide Tabela 1 – tempo 2), com mialgia intensa e perda da capacidade de deambular, sendo encaminhada para tratamento em hospital de referência para avaliação por especialista. Foi submetida à biópsia muscular, a qual apresentou padrão para dermatopolimiosite, sendo, assim, após a melhora da função hepática foi iniciada imunossupressão com metrotrexato. Em conseguinte, obteve melhora laboratorial (vide Tabela 1 - tempo 3) e clínica da sintomatologia referente à dermatopolimiosite. Segue em tratamento especializado e fisioterapia motora.
DISCUSSÃO
O Epstein-Barr vírus (EBV) é um DNA vírus da família Herpesviridae que está presente de forma latente em 95% da população mundial. É transmitido por gotículas de saliva que alcançam a faringe e infectam os linfócitos B. Este vírus promove uma infecção persistente com reativações periódicas na qual ocorre modulação da resposta imune humoral e celular do hospedeiro por meio da supressão da apoptose dos linfócitos B infectados, da forte resposta das células T CD8+ e da produção de imunomoduladores homólogos aos humanos, como IL-10 viral, que auxiliam na evasão imunológica1-3.
A infecção primária por EBV na infância geralmente é inaparente e atípica, apresentando quadro assintomático ou oligossintomático1,3,5. As manifestações clínicas típicas da mononucleose infecciosa são febre, faringite, adenopatia, fadiga, mialgia e artralgia, podendo apresentar também rash maculopapular generalizado, adenomegalia cervical, enantema palatino, edema periorbital, hepatoesplenomegalia e icterícia. O diagnóstico é clínico e confirmado por meio da sorologia através de anticorpos heterófilos ou por anticorpos anti-Epstein-Barr (IgM anti-VCA, IgG anti-VCA, IgG anti-EBNA, IgG anti-EA)1,5.
Esse vírus é suspeito de ser um forte fator ambiental na etiologia de doenças autoimunes, uma vez que suas proteínas virais estão envolvidas na alteração do sistema imune do hospedeiro, propiciando a perca da autotolerância e o desenvolvimento de neoplasias, como linfoma de Hodgkin1. Os mecanismos exatos pelos quais o EBV atua nas doenças autoimunes são desconhecidos, mas sugestiona-se que a mímica molecular por homologia entre as proteínas virais e as humanas desempenhe um forte papel em indivíduos geneticamente susceptíveis, fato exemplificado por estudos focados em anticorpos (anti-Sm B/B’, anti-Ro e anti-Sm D) relacionados ao lúpus eritematoso sistêmico (LES) que mostram reação cruzada entre as sequências peptídicas identificadas por esses anticorpos com a sequência peptídica da proteína viral EBNA-1 (reação cruzada entre os antígenos)2. Outra hipótese, é a interação genético-ambiental na qual as proteínas virais e seus fatores de transcrição humanos ocupam sítios genômicos de risco para doenças autoimunes, esse mecanismo é, também, observado no LES, no qual metade dos loci gênicos de risco realiza interseção com a proteína viral de fase latente EBNA-2. Ancorações similares ocorrem na esclerose múltipla, artrite idiopática juvenil, doença celíaca, entre outras6.
Entretanto, as evidências descrevem relação deste com apenas algumas doenças autoimunes: lúpus eritematoso sistêmico, síndrome de Sjögren, artrite reumatoide, miosite, miastenia gravis, artrite idiopática juvenil e esclerose múltipla1,2,6. Mas, apesar da literatura não demonstrar os mecanismos específicos da relação entre EBV e dermatopolimiosite, o vírus é um potencial agente etiológico e sugestiona-se que esse possua envolvimento na patogênese, pois é possível identificar, assim como nas outras doenças relacionadas acima, o aumento da carga viral e a predominância de anti-VCA nos indivíduos portadores de DM em comparação com indivíduos não portadores, além disso, é observada a melhora do quadro autoimune após tratamento efetivo contra o vírus, fato que apoia a hipótese1,2,4.
A dermatopolimiosite juvenil é uma miopatia inflamatória rara na infância caracterizada por fraqueza muscular e lesões cutâneas, resultantes da vasculite mediada por autoanticorpos e alterações mediadas por células como a inflamação linfocítica da musculatura esquelética e da pele7-9. Segundo a Sociedade Brasileira de Reumatologia, a DMJ possui prevalência maior no sexo feminino entre 4-10 anos e incidência de 0,4-0,5 pessoas acometidas para cada 100.000 habitantes nos Estados Unidos10. A etiologia é desconhecida, no entanto, evidências apontam a influência de fatores genéticos e ambientais, como a herança genética e as infecções virais8.
A DMJ apresenta-se inicialmente de forma inespecífica com evolução aguda ou crônica com febre, fadiga, mialgia, artralgia, anorexia e perda de peso. As primeiras manifestações comumente são lesões cutâneas, com edema e eritema em face, similar à lesão em asa de borboleta, e em regiões extensoras, as quais pioram com exposição ao sol7,9. Podem ter o eritema palpebral ou heliótropo e associação com o rash malar. O sinal de Gottron é considerado patognomônico, representado por lesões descamativas de coloração avermelhada sobre as articulações metacarpofalângicas e interfalângicas. A fraqueza muscular ocorre de forma proximal, bilateral, progressiva e simétrica com comprometimento da cintura escapular e pélvica. Além disso, a doença tem alterações multissistêmicas podendo a vasculite atingir órgãos internos, causando vômitos, síndrome da má absorção, dispneia, entre outros8.
Para o diagnóstico é fundamental excluir causas metabólicas, infecciosas e endócrinas7-9. Em seguida, é avaliada segundo os critérios de Bohan e Peter7, que se referem: 1) fraqueza muscular proximal das cinturas pélvica e escapular; 2) evidência de miosite à biópsia muscular; 3) elevação de qualquer enzima muscular sérica; 4) eletromiografia compatível com miopatia; 5) lesões cutâneas características de dermatomiosite.
A paciente do caso apresentou quadro de mononucleose com os sintomas típicos da doença: febre, faringite, adenopatia, mialgia, hepatoesplenomegalia e com os exames de sorologia para EBV (IgG e IgM) positivos e anticorpos heteróficos reagentes. Esta infecção piorou a situação oligossintomática em que a paciente se encontrava e desencadeou afloramento agudo do quadro de DMJ com manifestação das lesões cutâneas patognomômicas (sinal de Gottron), miosite e fraqueza muscular proximal e simétrica intensa, preenchendo, em conjunto com a biópsia muscular, quatro dos cinco critérios de diagnótico7 para dematopolimiosite. É importante ressaltar que a escolar se apresenta dentro das estatísticas epidemiológicas de sexo e idade para o desenvolvimento de DMJ9,10 e, além disso, possui herança familiar de doença autoimune.
Diante do exposto, sugestiona-se o envolvimento do EBV como fator etiológico na patogênese da dermatomiosite, uma vez que, assim como mostrado nos estudos, apresentou alta carga viral e a predominância de anti-VCA em concomitância à DMJ e, além disso, observou-se melhora com remissão do quadro viral1,2,4. Entretanto, é importante ressaltar que são necessárias mais pesquisas para o estabelecimento, com fortes evidências, de relações causais diretas entre o patógeno e esta doença autoimune.
CONCLUSÃO
Deve-se atentar para a influência do componente viral, como o Epstein-Barr vírus, na patogênese da dermatopolimiosite em indivíduos geneticamente predispostos a doenças autoimunes, fato que urge atenção médica para o correto manejo dessas infecções e acompanhamento posterior desses pacientes.
REFERÊNCIAS
1. Draborg AH, Duus K, Houen G. Epstein-Barr virus in systemic autoimmune diseases. Clin Develop Immun [Internet]. 2013 Jul; [acesso em 2019 Set 02]; 2013:535738. Disponível em: https://www.hindawi.com/journals/jir/2013/535738/ DOI: https://doi.org/10.1155/2013/535738
2. Ascherio A, Munger KL. EBV and autoimmunity. Curr Top Microbiol Immunol [Internet]. 2015 Out; [citado 2019 Set 01]; 390(Pt 1):365-85. Disponível em: https://link.springer.com/chapter/10.1007/978-3-319-22822-8_15 DOI: https://doi.org/10.1007/978-3-319-22822-8_15
3. Jog NR, Young KA, Munroe ME, Harmon MT, Guthridge JM, Kelly JA, et al. Association of Epstein-Barr vírus serological reactivation with transitioning to systemic lupus erythematosus in at-risk individuals. Ann Rheum Dis [Internet]. 2019 Jun; [citado 2019 Set 10]; 78(9):1235-41. Disponível em: https://www.ncbi.nlm.nih.gov/pubmed/31217170 DOI: https://doi.org/10.1136/annrheumdis-2019-215361
4. Huang PY, Zhong ZL, Luo DH, Mai HQ, Chen MY, Li YX, et al. Paired study of 172 cases of nasopharyngeal carcinoma with of without dermatomyositis. Acta Otolaryngol [Internet]. 2014 Ago; [citado 2019 Set 09]; 134(8):824-30. Disponível em: https://www.ncbi.nlm.nih.gov/pubmed/24909624 DOI: https://doi.org/10.3109/00016489.2014.913312
5. Aronson MD, Auwaerter PG. Infectious mononucleosis. UpToDate [Internet]. 2019 Mai; [acesso em 2019 Set 10]. Disponível em: https://www.uptodate.com/contents/infectiousmononucleosis/print?search=mononucleose&source=search_result&selectedTitle=1~150&usage_%E2%80%A6
6. Harley JB, Chen X, Pujato M, Miller D, Maddox A, Forney C, et al. Transcription factors operate across disease loci, with EBNA2 implicated in autoimmunity. Nat Genet [Internet]. 2018 Abr; [citado 2019 Set 10]; 50:699-707. Disponível em: https://www.nature.com/articles/s41588-018-0102-3 DOI: https://doi.org/10.1038/s41588-018-0102-3
7. Terreri MTSLRA. Dermatomiosite juvenil. In: Naspitz CK, Solé D, eds. Guia de alergia, imunologia e reumatologia em pediatria. 2ª ed. Barueri: Manole; 2012. p. 237-44.
8. Ministério da Saúde (BR). Portaria nº 1.692, de 22 de novembro de 2016. Protocolo Clínico e Diretrizes Terapêuticas da Dermatomiosite e Polimiosite. Diário Oficial da União, Brasília (DF). 2016 nov 25; 226: Seção 1: 39.
9. Hutchinson C, Feldman BM, Li SC, Patterson MC, TePas E. Juvenile dermatomyositis and polymyositis: Epidemiology, pathogenesis and clinical manifestations. UpToDate [Internet]. 2019 Ago; [acesso em 2020 Fev 02]. Disponível em: https://www.uptodate.com/contents/juvenile-dermatomyositis-and-polymyositis-epidemiology-pathogenesis-and-clinical-manifestations
10. Sociedade Brasileira de Reumatologia (SBR). Dermatomiosite. Orientações ao paciente [Internet]. São Paulo: SBR; 2011 Abr; [acesso em 2019 Set 04]. Disponível em: https://www.reumatologia.org.br/orientacoes-ao-paciente/dermatomiosite-juvenil
1. Universidade Potiguar, Medicina - Natal - RN - Brasil
2. Universidade Estadual do Rio Grande do Norte, Ciências médicas - Mossoró - RN - Brasil.
Endereço para correspondência:
Ana Clara Aragão Fernandes
Universidade Potiguar
Av. Sen. Salgado Filho, nº 1610,Lagoa Nova
Natal, RN, Brasil. CEP: 59056-000
E-mail: clara.aragao.wlj@hotmail.com
Data de Submissão: 29/03/2020
Data de Aprovação: 13/04/2020
Recebido em: 29/03/2020
Aceito em: 13/04/2020