A tuberculose (TB) é uma doença infecciosa grave, cuja incidência tem aumentado nos últimos anos1. Dados da Organização Mundial da Saúde (OMS) de 2018 mostram que aproximadamente 10 milhões de casos de TB e uma morte a cada 21 segundos são registradas todos os anos no mundo, sendo a doença infecciosa que mais mata jovens e adultos². Nesse mesmo ano, foram notificados aproximadamente 76 mil novos casos de TB e 4,5 mil mortes, estando o Brasil entre os vinte países com maiores incidências de TB3.
Além do sistema pulmonar, outros locais podem ser acometidos, como o sistema nervoso central (SNC), resultando na neurotuberculose. Nesse caso, a forma de acometimento mais frequente na infância é a meningoencefalite tuberculosa, complicação mais grave da doença4, responsável por quase metade do total de óbitos pelo acometimento neurológico no Brasil5. Assim, esta complicação é uma das mais temidas na infância, devido à morbimortalidade elevada e às sequelas neurológicas que costuma causar6.
Na clínica pediátrica o diagnóstico da TB ainda constitui um desafio, visto que as crianças podem apresentar sinais, sintomas e alterações radiológicas inespecíficas. Além disso, nesta faixa etária, o isolamento do bacilo de Koch é difícil7, sendo preconizado o diagnóstico por meio de um sistema de pontuação8. Porém, isso contribui para subnotificação da TB infantil9, que mesmo subestimada é responsável por 10% do total de casos10. Soma-se a isso a pouca atenção dada à TB pelos programas de saúde infantil9, o que favorece diagnósticos tardios associados a danos neurológicos irreversíveis11.
RELATO DE CASO
História clínica: lactente, masculino, 3m e 16d, previamente hígido e com cicatriz vacinal de BCG. Internado em 16/07/17 devido a quadro de tosse e febre não aferida há 10 dias, irresponsivo a amoxicilina-clavulanato. Em 19/07/17, apresentou febre noturna e sudorese profusa. Radiografia de tórax evidenciou padrão miliar bilateral. Dados epidemiológicos: cuidadora do bebê em tratamento para TB. Teste tuberculínico reator fraco, lavado gástrico para pesquisa do bacilo álcool-ácido resistente (BAAR) e testes anti-HIV I e II negativos. Totalizou-se 40 pontos no escore diagnóstico proposto pelo Ministério da Saúde (MS)12. Foi indicado esquema tríplice (2RHZ/4RH) com rifampicina, izoniazida e pirazinamida. Recebeu alta hospitalar em 28/07/17, após melhora clínica, e foi encaminhamento para seguimento ambulatorial na rede SUS.
Em 21/08/17, mãe relatou suspensão dos antituberculínicos por outro profissional devido à hepatotoxicidade (TGO:191/TGP:179). Com a redução dos níveis séricos das enzimas hepáticas (TGO:43,3/TGP:27), houve reintrodução da rifampicina. Foram realizados novos exames (TGO:33,9/TGP:14,7/GGT:33,6). Em 22/08/17, a isoniazida foi reintroduzida. Após 1 semana, houve novo controle laboratorial e associação da pirazinamida ao tratamento.
Nova internação em 09/09/17, após comparecer ao pronto atendimento com relato materno de “desvio no olhar”. Ao exame: bom estado geral, estável hemodinamicamente, murmúrio vesicular audível e rude, sem ruídos adventícios. Fontanela anterior normotensa e ausência de rigidez nucal. Pupilas isocóricas e fotorreagentes. Exame neurológico detectou estrabismo convergente bilateral e paralisia facial à direita. Hipóteses: acometimento neurológico pela TB ou neuropatia pela isoniazida. Tomografia computadorizada (TC) de crânio com contraste evidenciou lesões hipodensas focais e edema do parênquima cerebral, com realce anelar, sinais compatíveis com neurotuberculose (Figura 1). Associados aos antituberculínicos, foram prescritos dexametasona EV (0,4mg/kg/dia) e piridoxina (50mg/dia), ambos por 7 dias, e foi iniciada fisioterapia motora precoce. Lactente permaneceu estável, com enzimas hepáticas controladas e melhora da paralisia facial e do aspecto miliar na radiografia de tórax. Alta hospitalar em 19/09/17, com orientação para seguimento ambulatorial. Mantido o esquema tríplice + prednisolona, com tempo de tratamento ampliado para 9 meses, conforme preconizado para a TB meningoencefálica (2RHZ/7RH) pelas diretrizes vigentes em 2017. Após um mês, retornou às consultas assintomático e com significativa regressão do quadro radiológico. Seguiu em domicílio, sem complicações e com acompanhamento por pediatra, oftalmologista, neurologista e fisioterapeuta.
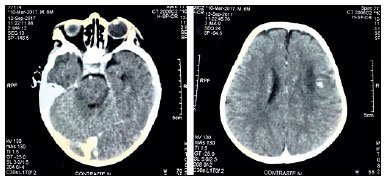 Figura 1. Tomografia computadorizada de crânio (TC neurotuberculose).
Figura 1. Tomografia computadorizada de crânio (TC neurotuberculose).A TB miliar constitui uma forma grave da doença, acometendo mais frequentemente pacientes imunocomprometidos12. O envolvimento do SNC é mais comum em crianças com idade entre seis meses e seis anos. Nesses casos, formam-se granulomas, principalmente submeníngeos, decorrentes da disseminação hematogênica a partir do foco primário pulmonar4,6. Esses granulomas podem levar à descarga de conteúdo caseoso para as meninges, podendo ocasionar: 1) obstrução da passagem liquórica pelas cisternas, gerando hidrocefalia; 2) comprometimento de nervos cranianos e do quiasma óptico, causando paresias, paralisias e amaurose; e, 3) envolvimento das artérias carótida interna e cerebral média, comprometendo a irrigação parenquimatosa. Podem ser observados ainda edema tecidual e vasculite por reação de hipersensibilidade ao antígeno, contribuindo para a ocorrência de sequelas neurológicas6.
Os sinais e sintomas do acometimento neurológico podem ser inespecíficos, sendo o diagnóstico muitas vezes tardio; isso dificulta o tratamento e está associado a piores prognósticos6. Quando sintomática, pode ocorrer febre e síndrome de hipertensão intracraniana, com cefaleia, náuseas, vômitos, confusão mental e coma. A confirmação diagnóstica baseia-se, principalmente, na análise do líquido cefalorraquidiano (LCR) e exames de imagem13. O primeiro exame a ser realizado deve ser tomografia computadorizada (TC) ou ressonância magnética (RM) com contraste. Os achados mais comuns são: hidrocefalia, espessamento meníngeo basal e infartos do parênquima cerebral12.
Na análise do LCR (não realizada), observa-se pleocitose, leucocitose com predomínio linfocitário, proteínas elevadas e glicose baixa. A pesquisa do BAAR é positiva em 5-20% dos casos. Já a cultura é positiva em metade dos casos14,15. Atualmente, a técnica de PCR é um dos principais métodos para detecção da meningoencefalite tuberculosa13. Assim, o diagnóstico é realizado pela avaliação clínico-radiológica associada à baciloscopia, cultura de escarro e testes de biologia molecular quando possível. O diagnóstico diferencial deve ser feito com infecções bacterianas, fúngicas ou virais do SNC, bem como outras causas de meningite. O diagnóstico radiológico diferencial inclui criptococose, sarcoidose, linfomas, metástases e encefalite por citomegalovírus12.
Como tratamento da TB menigoencefálica em crianças <10 anos de idade, é recomendado atualmente pelo MS o esquema 2RHZ/10RH. Esse tratamento é dividido em fases intensiva e de manutenção, e os esquemas preconizados pelo manual de 2011 e 2019 diferem somente pela duração da fase de manutenção (Tabela 1). Assim, no caso apresentado, o lactente foi tratado com o esquema 2RHZ/7RH (totalizando 9 meses) devido ao manual vigente em 201716,17. Na fase intensiva, há a associação de corticosteroides, para atenuar a resposta inflamatória ao antígeno e auxiliar no tratamento das complicações15. As principais reações adversas, apesar de raras na criança, devem ser informadas à família. Além disso, deve-se orientar sobre o seguimento clínico.

A hepatotoxicidade é um evento adverso frequente em formas graves de TB, sendo recomendado realizar prova de função hepática antes de iniciar o tratamento, com monitoração periódica (a cada 3-7 dias). Se houver elevação ≥5 vezes o limite superior da normalidade (LSN) em pacientes assintomáticos, ou 3 vezes o LSN com sintomas dispépticos, ou presença de icterícia, deve-se suspender o tratamento. A reintrodução dos medicamentos deverá ser feita gradualmente, após avaliação da função hepática, da seguinte forma: RE, seguidos de H e por último a Z 12. Outras preocupações são as sequelas neurológicas, como déficits motores, retardo do desenvolvimento ou demência, síndromes convulsivas e hidrocefalia15.
Quanto mais precocemente o tratamento medicamentoso e a fisioterapia forem instituídos, melhor a evolução e recuperação do paciente. Na TB pulmonar, vários fatores podem influenciar a evolução clínica: idade, presença de tuberculose extra-meníngea, vacinação com BCG, alterações liquóricas, hipertensão intracraniana, alteração do nível de consciência, déficits neurológicos, tipo de esquema de tratamento utilizado, uso de corticosteroides e outras comorbidades12,15.
Por fim, durante o tratamento, o seguimento clínico deve ser mensal e multidisciplinar, acompanhado de exame bacteriológico quando possível. Na criança, é importante lembrar o ajuste de doses do esquema terapêutico de acordo com o ganho de peso. O controle radiológico deve ser realizado no segundo mês de tratamento (caso a evolução seja favorável) ou no primeiro mês (caso a evolução seja desfavorável), bem como ao término do tratamento. A melhora clínica e radiológica são os principais critérios para avaliação de cura12.
CONCLUSÃO
A TB miliar constitui apresentação grave da doença na infância, com risco de acometimento meníngeo por disseminação hematogênica. Em caso de acometimento neurológico, o tratamento geralmente requer tempo de internação e tratamento prolongados, com acompanhamento multidisciplinar. Ressalta-se que a investigação do acometimento do SNC deve sempre ser considerada no momento do diagnóstico, sobretudo no Brasil, onde existe uma alta prevalência de TB. Portanto, é essencial o diagnóstico e tratamento precoces, bem como ações de prevenção, a fim de reduzir a ocorrência de formas graves e a morbimortalidade das crianças acometidas.
AGRADECIMENTOS
Agradecemos ao grupo de pesquisa “Qualidade de Vida e Epidemiologia” da Universidade Federal de São João Del Rei (UFSJ) - Campus Dom Bosco, orientado pela Profª. Drª. Jacqueline Domingues Tibúrcio e com colaboração da Profª. Márcia Reimol de Andrade.
REFERÊNCIAS
1. Ministério da Saúde (BR). Secretaria de Vigilância em Saúde. Departamento de Vigilância das Doenças Transmissíveis. Brasil livre da tuberculose: plano nacional pelo fim da tuberculose como problema de saúde pública. Brasília (DF): Ministério da Saúde; 2017.
2. World Health Organization (WHO). Global tuberculosis report 2019 [Internet]. Geneva: WHO; 2019; [acesso em 2020 Jun 10]. Disponível em: https://www.who.int/tb/publications/global_report/en/
3. Conselho Federal de Medicina (CFM). Brasil é o 20º país com maior incidência de tuberculose e enfrenta desafios [Internet]. Brasília: Portal CFM; 2017; [acesso em 2018 Jul 20]. Disponível em: https://portal.cfm.org.br/index.php?option=com_content&view=article&id=26873:2017-04-20-18-02-48&catid=3
4. Xavier CC, Carvalho LFA, Abrantes MM, Melo RP. Neurotuberculose na infância. Rev Med Minas Gerais. 2003;13(3):211-4.
5. Ministério da Saúde (BR). Secretaria de Vigilância em Saúde. Departamento de Vigilância das Doenças Transmissíveis. Panorama da tuberculose no Brasil: a mortalidade em números. Brasília (DF): Ministério da Saúde; 2016.
6. Gusmão Filho FAR, Marques HHS, Dias MJ, Ramos RTS. Tuberculose do sistema nervoso central em crianças: apresentação clínica e laboratorial. Arq Neuro-Psiquiatr. 2001 Mar;59(1):71-6.
7. Schmidt CM, Queiroz A, Cardoso CAA. Utilização de biomarcadores na tuberculose pediátrica. Resid Pediatr. 2017;7(Supl 1):S32-S7. DOI: https://doi.org/10.25060/residpediatr-2017.v7s1-08
8. March MFBP, Aurílio RB. Diagnóstico laboratorial da tuberculose na infância. Resid Pediatr. 2017;7(Supl 1):S27-S31. DOI: https://doi.org/10.25060/residpediatr-2017.v7s1-07
9. Starke JR. Childhood tuberculosis in 2017: where do we go from here? Resid Pediatr. 2017;7(Supl 1):S3-S6.
10. Carvalho ACC, Cardoso CAA, Martire TM, Migliori GB, Sant’Anna CC, et al. Aspectos epidemiológicos, manifestações clinicas e prevenção da tuberculose pediátrica sob a perspectiva da Estratégia End TB. J Bras Pneumol. 2018;44(2):134-44.
11. Newton RW. Tuberculous meningitis. Arch Dis Child 1994; 70: 364-366.
12. Brasil. Ministério da Saúde. Secretaria de Vigilância em Saúde. Departamento de Vigilância Epidemiológica. Manual de recomendações para o controle da tuberculose no Brasil [Online]. 2ª ed. Brasília: 2019. [acesso 2020 Jun 10] Disponível em: HYPERLINK “https://bvsms.saude.gov.br/bvs/publicacoes/manual_recomendacoes_controle_tuberculose_brasil_2_ed.pdf” https://bvsms.saude.gov.br/bvs/publicacoes/manual_recomendacoes_controle_tuberculose_brasil_2_ed.pdf
13. Canoa APG, Romanelib MTN, Pereirac RM, Tresoldic AT. Tuberculose em pacientes pediátricos: como tem sido feito o diagnóstico? Rev. paul. pediatr. 2017; 35(2): 165-70.
14. Conde MB, Melo FA, Marques AMC, Cardoso NC, Pinheiro VGF, Dalcin PTR, et.al. Diretrizes para Tuberculose da Sociedade Brasileira de Pneumologia e Tisiologia. J. bras. pneumol. 2009; 35(10).
15. Canoa APG, Romanelib MTN, Pereirac RM, Tresoldic AT. Tuberculose em pacientes pediátricos: como tem sido feito o diagnóstico? Rev. paul. pediatr. 2017; 35(2): 165-70.
16. Gusmão FAR, Marques HHS, Dias MJM, Ramos SRTS. Tuberculose do sistema nervoso central em crianças: tratamento e evolução. Arq. Neurop. 2001; 59(1): 77-82.
17. Brasil. Ministério da Saúde. Secretaria de Vigilância em Saúde. Departamento de Vigilância Epidemiológica. Manual de Recomendações Para o Controle da Tuberculose no Brasil [Online]. Brasília: 2011 [acesso 2020 Jun 10]. Disponível em: http://bvsms.saude.gov.br/bvs/publicacoes/manual_recomendacoes_controle_tuberculose_brasil.pdf
Universidade Federal de São João Del Rei, Medicina - São João del-Rei - Minas Gerais - Brasil
Endereço para correspondência:
Márcia Reimol de Andrade
Universidade Federal de São João del-Rei
Praça Frei Orlando, nº 170,Centro, São João del-Rei
Minas Gerais, Brasil. CEP: 36307-352
E-mail: mmreimol@ufsj.edu.br
Data de Submissão: 13/05/2020
Data de Aprovação: 24/06/2020
Recebido em: 13/05/2020
Aceito em: 24/06/2020


